Гастроинтестинальная стромальная опухоль
Среди всех злокачественных образований желудочно-кишечного тракта на гастроинтестинальные стромальные опухоли приходится примерно 1%. В случае этого редкого заболевания определенные надежды возлагаются на таргетную терапию мультикиназным ингибитором (стиварга). В этой статье будут рассмотрены причины появления такой патологии, ее классификация, симптомы, диагностика, лечение и прогноз жизни.
Что такое гастроинтестинальные стромальные опухоли
Гастроинтестинальная стромальная опухоль (ГИСО, GIST) — мезенхимальное образование злокачественной природы. Имеется предположение, что она развивается из клеток Кахала или их предшественников.
Такая опухоль имеет сходство с гладкомышечными и нейрогенными образованиями. Однако при более глубоком исследовании у нее выявляются определенные особенности, позволяющие отнести эти новообразования в отдельную группу.
Важно! Все виды ГИСО потенциально злокачественные и метастазируют преимущественно гематогенным путем.
GIST — это узел, локализованный под слизистой. Такие образования склонны расти в просвет полого органа. Насколько опухоль опасна, зависит от ее расположения, размера и скорости деления.
У ГИСО, размер которой не превышает 2-5 см, злокачественный потенциал довольно низкий, а у образований диаметром более 10 см он заметно выше.
В каждом клиническом случае подбирается своя тактика терапии GIST. Обязательным аспектом лечения является поиск мутаций в генах. При их выявлении прибегают к таргетной терапии с использованием низкомолекулярных ингибиторов тирозинкиназ и мультикиназного ингибитора. Такое лечение проводят в несколько стадий.
Классификация гастроинтестинальных стромальных опухолей
ГИСО присвоены следующие коды по МКБ-10 (Международная классификация болезней 10-го пересмотра): С15-С20, а также С48.0 и С48.01. Общее название — злокачественные новообразования органов пищеварения.
Согласно коду по МКБ 10, гастроинтестинальные стромальные опухоли затрагивают разные отделы ЖКТ:
- С15 — пищевода;
- С16 — желудка;
- С17.0 — двенадцатиперстной кишки;
- С17.2 — среднего отдела тонкой кишки;
- С17.3 — подвздошной кишки;
- С18 — основного отдела толстого кишечника;
- С19 — ректосигмоидного соединения ободочной кишки;
- С20 — прямой кишки;
- С48.0 — ретроперитонеального пространства;
- С48.1 — уточненные части брюшины (брыжейки, большого и малого сальников).
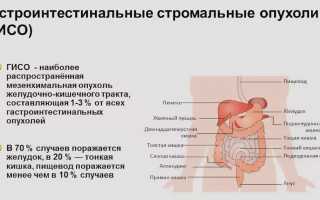
Частота развития GIST в различных отделах пищеварительного тракта разнится: в желудке — 60%, в тонкой кишке — 25%, в толстой кишке — 8%, в прямой кишке — 5%, в пищеводе — 2%. Другие отделы страдают от такой патологии еще реже.
Согласно гистологической классификации, эти опухоли бывают трех видов:
- веретеноклеточные;
- эпителиоидноклеточные;
- смешанные.
В 70 % случаев диагностируют веретеноклеточные стромальные новообразования. Согласно современной концепции, все гастроинтестинальные стромальные опухоли считаются потенциально злокачественными, но с разной вероятностью.
Причины стромальных опухолей
В большинстве случаев гастроинтестинальные стромальные опухоли появляются спонтанно. До 85 % ГИСО имеют мутации в гене C-KIT и 3-18 % — в гене PDGFRA. В 10-15% случаев мутации в этих генах не выявляют, поэтому патологии присваивается дикий тип (WT).
Но более широкие генетические исследования доказывают, что стромальные опухоли с WT — это разнородная группа, у которой присутствует активирующая мутация ряда генов.
Справка! Гораздо реже ГИСО возникает в рамках наследственных семейных или идиопатических мультиопухолевых синдромов (триада Карнея).
Симптомы гастроинтестинальных стромальных опухолей
GIST не имеет специфических проявлений. На ранних стадиях у большинства стромальных опухолей симптомы отсутствуют. Даже довольно большие образования данного типа часто никак не дают о себе знать.
Но со временем, как и при других злокачественных опухолях ЖКТ, у пациентов появляются: абдоминальные боли, тошнота, беспричинная потеря веса, повышенная утомляемость.
На слизистой оболочке, под которой находится опухоль, может появиться язва, провоцирующая скрытое или массивное кровотечение в ЖКТ. Это приводит к развитию гематологического синдрома, характеризующегося нарушением синтеза гемоглобина на фоне недостатка железа.
Опухоль желудка, локализованная в области антрума, может спровоцировать патологическое сужение выходного отдела этого органа.
Диагностика ГИСО
Перед любыми лечебными воздействиями при подозрении на гастроинтестинальные стромальные опухоли проводят тщательную диагностику:
- Внимательно собирают жалобы и анамнез, а также выполняют физикальный осмотр.
- Делают расширенный общий и биохимический анализ крови.
- Проводят эндоскопическое обследование. Это может быть классическая ЭГДС или более информативное ультразвуковое эндоскопическое исследование.
- Выполняют КТ органов брюшной полости с контрастом. Этот метод оптимален как при первичных опухолях, так и при наличии отдаленных вторичных очагов патологического процесса. Альтернативный метод — УЗИ органов брюшной полости и малого таза. Но по информативности оно сильно уступает КТ.
- При наличии удаленной опухоли или тканей, добытых путем биопсии, проводят морфологическое исследование. В гистологическом заключении обычно указывают: размер опухоли, ее расположение, клинико-морфологические особенности, митотический индекс. Также отмечают, имел ли место разрыв капсулы опухоли.
- Выполняют ИГХ с определением экспрессии CD117 и/или DOG1. Если опухоль оказывается негативной относительно CD117 и DOG1, то выполняют молекулярно-генетический анализ.
- Определяют мутации в генах KIT (экзоны 9, 11), PDGFRA (экзоны 12, 14, 18, D842V) или констатируют их отсутствие в случае дикого типа ГИСО.
- При опухолях прямой кишки выполняют УЗИ малого таза. Более точную информацию об этом отделе получают, если проводят МРТ с контрастом.
- При неубедительных результатах классической КТ или для оценки эффективности терапии прибегают к ПЭТ.
Если имеется подозрение на стромальную опухоль, то использование компьютерной томографии — это основной диагностический стандарт.
А проводить core-биопсию (чрезкожная пункционная манипуляция) под контролем УЗИ при опухолях такого типа нежелательно, поскольку такая процедура может спровоцировать разрыв капсулы новообразования и диссеминацию онкологического процесса по брюшине или по ходу пункционного канала.
Если у пациентов особо сложный случай (возникли трудности при постановке молекулярно-генетического диагноза, выявлена триада Карнея или дикий тип GIST), то дополнительные обследования и терапию осуществляют в специализированных онкологических учреждениях.
Справка! Примерно 20% GIST случайно обнаруживаются при проведении стандартного рентгена желудка с контрастом или ЭГДС в сочетании с эндоскопическим ультразвуком.
Лечение гастроинтестинальных стромальных опухолей
При четкой, нерассеянной локализации гастроинтестинальных стромальных опухолей лечение начинают с хирургического вмешательства. При нерезектабельных образованиях, возобновлении болезни после ремиссии или при наличии метастазов отдают предпочтение таргетной терапии.
Локализованные формы
При новообразованиях малых размеров (менее 1-2 см), если позволяет клиническая ситуация, оправдано наблюдение за пациентом в динамике.
Однако, отказавшись от активной хирургической тактики, необходимо учитывать потенциальный риск прогрессирования патологии, опираясь на гистологические исследования. Если образовании более 2 см, то показано радикальное вмешательство.
Нюансы терапии с применением хирургических методов:
- При расположении опухоли в пищеводе, входном отделе желудка, 12-перстной или прямой кишке, перед резекцией рекомендована терапия, позволяющая уменьшить ее размеры. А затем выполняют операцию с сохранением органа.
- Если есть сомнения относительно операбельности опухоли, то перед запланированным радикальным вмешательством рекомендовано на протяжении 6-12 месяцев принимать иматиниб.
- За пациентами с низким риском прогрессирования патологии, после хирургического вмешательства осуществляют динамическое наблюдение. Если риск высокий или промежуточный, то прибегают к лекарственной терапии иматинибом на протяжении 1-3 лет.
После полного курса адъювантной терапии, в случае рецидива болезни, снова возобновляют прием иматиниба.
Диссеминированные опухоли и другие случаи
При диссеминированных случаях ГИСО или при отсутствии возможности выполнить резекцию, последовательно проводят 3 линии таргетной терапии:
- Иматиниб — это препарат первой линии. Он представляет собой низкомолекулярный ингибитор ряда рецепторных (с-KIT, PDGFRα) и не рецепторных тирозинкиназ (Abl, Bcr-Abl). Не исключено развитие первичной или вторичной резистентности к этому веществу.
- Сунитиниб — это препарат второй линии. Он относится к низкомолекулярным ингибиторам различных (более 80) тирозинкиназ. Однако из-за выраженной токсичности некоторые больные прерывают лечение этим веществом.
- Регорафениб — это препарат третьей линии. Это пероральный мультитаргетный (мультикиназный) ингибитор, действующий на тирозинкиназы, ангиогенез и микроокружения опухоли. Регорафениб назначается пациентам, которые были вынуждены прекратить прием сунитиниба из-за его непереносимости.
В большинстве рассеянных случаев ГИСО развивается устойчивость к иматинибу и сунитинибу, на фоне которой болезнь начинает динамично прогрессировать.
Регорафениб — это основное решение проблемы, если первые 2 препарата перестают себя оправдывать. Благодаря этому больные получают продолжительную, успешную терапию.
Обычно лечение начинают с применения иматиниба, постепенно заменяя дозировку 400 мг на 800 мг в сутки. На следующем этапе переходят к сунитинибу и лишь затем к регорафенибу.
Однако, при повышенной чувствительности к сунитинибу, уже во второй линии возможно применение регорафениба, оказывающего меньшую токсичность на организм.
Прогноз жизни
Для прогнозирования продолжительности жизни больного учитывают индекс митотической активности, расположение и величину первичной опухоли. Также ряд исследований выявил взаимосвязь между характером мутации с-KIT и качеством, продолжительностью жизни пациентов без рецидивов.
После операбельного вмешательства больные живут еще на протяжении 5 лет в 35-65% случаев.
При возобновлении болезни после ремиссии или при диагностированном диссеминированном или неоперабельном процессе пациенты обычно живут не более 10-20 месяцев.
Даже при удалении образований, возникающих при рецидиве, выживаемость больных не становится намного лучше. После повторной операции жизнь пациентов продолжается еще максимум 15 месяцев.
Заключение
Небольшие образования GIST чаще всего не проявляются клинически. Они становятся случайными находками в результате лечебных или диагностических манипуляций, проводимых по другим причинам.
Если процесс не диссеминированный, то в приоритете хирургическое лечение. В настоящее время больные ГИСО могут получать успешную длительную терапию, включая мультикиназные ингибиторы. Прогноз в различных клинических случаях существенно отличается.